این بخش شامل قسمت های زیر است:
15- شیمی سبز
16- هیدروژن و توسعۀ پایدار
17- اوزون
15- شیمی سبز
| دانلود جزوه تمامی فرمول های شیمی |
شیمی سبز شاخهای از شیمی است که در آن شیمیدان ها در جستجوی فرایندها و فرآورده هایی هستند که به کمک آن ها بتوان کیفیت زندگی را با بهرهگیری از منابع طبیعی افزایش داد و همزمان از طبیعت محافظت کرد. به همین منظور باید تولید و مصرف مواد شیمیایی را که ردپاهای سنگینی روی کره زمین برجا میگذارد، کاهش داد یا متوقف کرد.
برخی از دستاوزدهای شیمی سبز عبارتند از:
1- تولید سوخت سبز

2- تبدیل CO2 به مواد معدنی
برای این منظور، کربن دی اکسید تولید شده در نیروگاه ها و مراکز صنعتی را با منیزیم اکسید یا کلسیم اکسید واکنش می دهند.
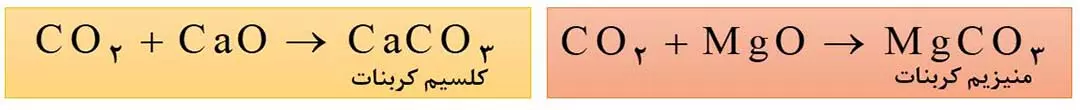
3- تولید پلاستیک سبز

4- دفن کردن کربن دی اکسید
کربن دی اکسید را می توان به جای رها کردن در هواکره، در مکان های عمیق و امن در زیر زمین ذخیره و نگهداری کرد.

5- تولید خودرو و سوخت با کیفیت بسیار مطلوب

16- هیدروژن و توسعۀ پایدار
هیدروژن فراوان ترین عنصر موجود در جهان است که به صورت ترکیب های گوناگون یافت میشود. این گاز مانند سوختهای فسیلی می تواند با اکسیژن بسوزد و نور و گرما تولید کند:
2H2+O2—–>2H2O
بر اثر سوختن سوخت های فسیلی، آلاینده هایی مانند CO2 ، CO ، SO2 و NO2 تولید می شود؛ بنابراین می توان گفت استفاده از گاز هیدروژن در مقایسه با سوخت های فسیلی آلاینده های کم تری ایجاد می کند.
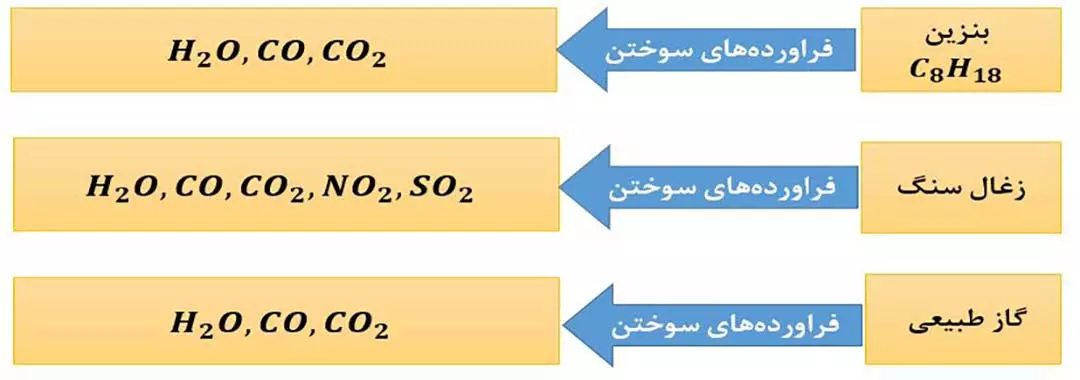
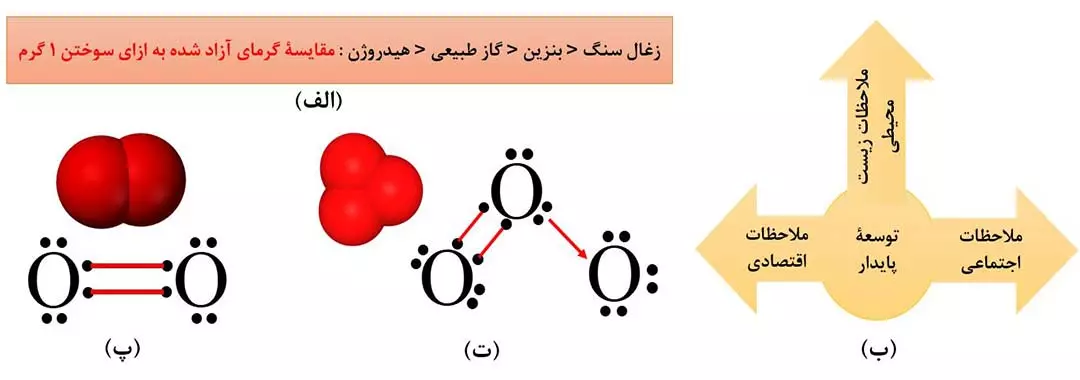
با اینکه تولید، حمل و نقل و نگهداری هیدروژن بسیار پرهزینه است، ولی بر اساس مفهوم «توسعۀ پایدار»، تولید این گاز صرفه اقتصادی دارد. توسعۀ پایدار یعنی اینکه در تولید هر فراورده، همۀ هزینه های اقتصادی، اجتماعی و زیست محیطی آن در نظر گرفته شود. بر این اساس هرگاه در مجموع شرکت ها و کارخانه ها، کالاهایی را تولید کنند که قیمت تمام شدۀ تولید کالا (از هر جهت) برای کشور کاهش یابد، این توسعه باعث رشد واقعی کشور می شود و در طولانی مدت باعث حفظ یا کاهش مصرف منابع طبیعی می شود.
17- اوزون
آ) مقایسۀ خواص اوزون ( O3 ) با اکسیژن ( O2 )
به شکل های گوناگون مولکولی با بلوری یک عنصری آلوتروپ یا دگرشکل می گویند. به طور مثال عنصر اکسیژن به دوصورت گاز اکسیژن (O2) و گاز اوزون (O3) در هواکره یافت می شود؛ پس از اکسیژن دارای دو آلوتروپ است.
آرایش الکترون_ نقطه ای (ساختار لوویس) و مدل فضا پرکن مولکول های اکسیژن و اوزون را در ( شکل 7 – پ و 7 ت ) مشاهده کنید.
همانطور که میبینید شمار جفت الکترون های پیوندی و ناپیوندی در اوزون بیشتر از اکسیژن است، اما نسبت شمار جفت الکترون های ناپیوندی به پیوندی در دو مولکول، یکسان و برابر با ۲ است.
توجه: سه اتم اکسیژن در مولکول اوزون روی یک خط راست قرار ندارند. به عبارت دیگر مولکول اوزون خمیده (V شکل) است.
- اوزون و اکسیژن در حالت مایع، آبی رنگ هستند.
- جرم مولی گاز اوزون (O3)، 1/5 برابر جرم مولی گاز اکسیژن (O2) است.
- با توجه به مطالب فصل سوم، خواهیم فهمید که O3 برخلاف O2 قطبی است؛ بنابراین می توان گفت انحلال پذیری اوزون در آب بیشتر می باشد.
- نقطه جوش گاز اوزون از گاز اکسیژن بیشتر است؛ بنابراین با سرد کردن این دو گاز، اوزون راحت تر به مایع تبدیل می شود.
- اوزون از اکسیژن واکنش پذیرتر است و در صنعت از گاز اوزون، برای گندزدایی میوه ها، سبزیجات و از بین بردن جانداران ذره بینی درون آب استفاده می شود.
توجه: با توجه به اختلاف رفتار اکسیژن و اوزون میتوان گفت: «ساختار هر ماده تعیین کننده خواص و رفتار آن است.»
ب) نقش محافظتی اوزون در لایۀ استراتوسفر
- لایۀ اوزون: منطقهای مشخصی از استراتوسفر است که بیشترین مقدار اوزون در آن محدوده قرار دارد. حواسمان باشد! که به طور کلی مقدار اوزون در هواکره ناچیز است.
- مولکول های اوزون در استراتوسفر نقش مفید و محافظتی دارند؛ به طوری که مانع ورود بخش عمدهای از تابش فرابنفش خورشید به سطح زمین می شود.
هنگامی که تابش پر انرژی فرابنفش به مولکولهای O3 در لایه اوزون برخورد می کند O3 می شکند. و به یک اتم اکسیژن (O) و یک مولکول اکسیژن (O2) تبدیل می شود. (شکل 8 – الف)
ذره های تولید شده (O و O2) دوباره با هم واکنش می دهند و مولکول اوزون را به وجود می آورد. بر اثر انجام این واکنش، مقداری انرژی به صورت تابش فروسرخ آزاد می شود. (شکل 8 – ب)
با تکرار پیوسته این دو واکنش ( شکل 8 – الف و ب )، لایۀ اوزون بخش قابل توجهی از تابش پر انرژی فراوانی را جذب و تابش کم انرژی تر فروسرخ را به زمین گسیل می دارد.

واکنش ها را می توان به دو دسته واکنش های برگشت ناپذیر (یک طرفه) و واکنشهای برگشت پذیر (دوطرفه) تقسیم کرد.
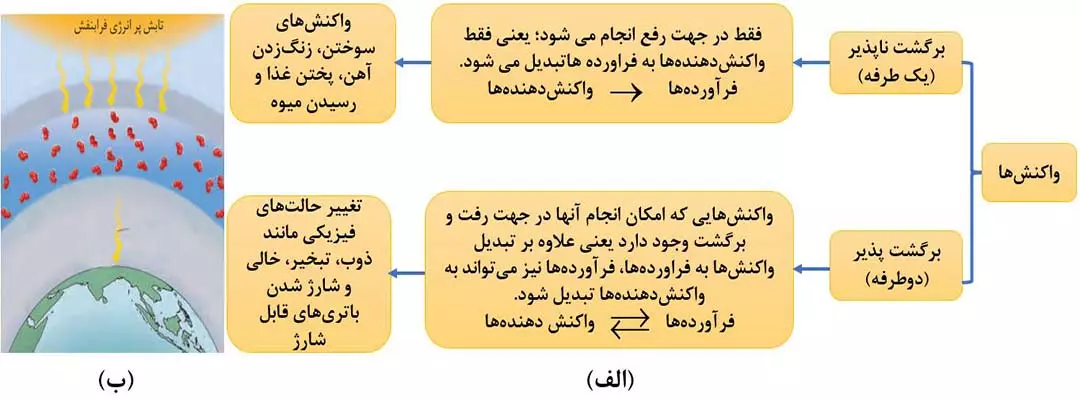
مجموعۀ واکنش های لایۀ اوزون را می توان با معادلۀ (شکل 8-پ) نشان داد. به عبارت دیگر واکنش تبدیل اوزون به اکسیژن، نمونۀ یک واکنش برگشت پذیر است. با توجه به برگشت پذیر است. با توجه به برگشت پذیر بودن این واکنش می توان گفت غلظت اوزون در استراتوسفر ثابت می ماند.
پ) اوزون تروپوسفری
- اوزون علاوه بر لایۀ استراتوسفر، در لایۀ تروپوسفر نیز یافت می شود. این گاز در لایۀ تروپوسفر آلاینده ای سمی است؛ به طوری که وجود آن در هوایی که تنفس می کنیم، سبب سوزش چشمان و آسیب دیدن ریه ها می شود.
- اوزون تروپوسفری از واکنش گاز قهوه ای رنگ نیتروژن دی اکسید با گاز اکسیژن در حضور نور خورشید تولید می شود. (شکل 10-الف)
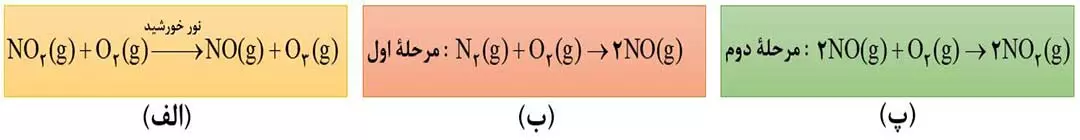
سوال: NO2 از کجا می آید؟
- گاز نیتروژن به عنوان اصلی ترین جز سازندۀ هواکره، واکنش پذیری بسیار کمی دارد به طور معمول با اکسیژن واکنش نمی دهد؛ اما بر اثر رعد و برق و بالا رفتن دما، با اکسیژن هوا واکنش داده و طی دو مرحله به NO2 تبدیل می شود.(شکل 10-ب و پ)
- در هوای آلودۀ شهرهای صنعتی و بزرگ، مقدار زیادی اکسیدهای نیتروژن وجود دارد. در واقع این گازها، از واکنش گازهای نیتروژن و اکسیژن درون موتور خودرو در دمای بالا به وجود می آیند.
پایان بخش 4 فصل 2 آموزش خط به خط شیمی دهم. کاری از سایت تدریس خصوصی استادلینک. با تشکر از دکتر آینده جناب محمدرضا احسان دوست
مقالات مرتبط فصل2 شیمی1
فصل2 – بخش صفر – اهمیت شیمی در کنکور سراسری
فصل2 – بخش اول – هواکره – تقطیر جزء به جزء هوای مایع
فصل2 – بخش دوم – اکسیژن – موازنۀ واکنش های شیمیایی
فصل2 – بخش سوم – ساختار لوویس – اثر گلخانه ای – اکسیدهای فلزی و نافلزی
فصل2 – بخش پنجم – قانون آووگادرو – شرایط STP – قانون ترکیبی گازها






